Il successo economico e la sostenibilità della produzione suinicola è strettamente collegata all'efficienza alimentare. Una delle vie più effiaci per migliorare l'efficienza alimentare è aumentare la deposizione di massa magra nei suini. L'evoluzione della definizione dei fabbisogni nutrizionali dei suini e la selezione genetica per il miglioramento degli accrescimenti hanno permesso un avanzamento spettacolare sulla conversione alimentare negli ultimi 20 anni. Con il progredire dei miglioramenti tecnologici nell'analizzare l'espressione globale dei geni, è aumentato l'interesse verso la nutrizione associata alla genetica. La genomica, conosciuta anche come nutrigenomica, studia sia i fabbisogni specifici per un dato tipo genetico sia le interazioni tra nutrienti e geni. Comprendere le complesse interazioni tra nutrizione e genetica su cui si basa l'efficienza energetica è fondamentale per identificare nuovi interventi che portino ad una maggior sostenibilità della produzione suinicola. L'applicazione della nutrigenomica nei suini giovani è particolarmente importante, dato che gli accrescimenti post-svezzamento e fase successiva sono buoni predittori degli accrescimenti su tutta la vita produttiva del soggetto (Main et al., 2004).

Nutrigenomica e accrescimenti
Lo sviluppo del tessuto muscolare, adiposo ed osseo è correlato e regolato in modo dinamico dalla nutrizione mediante cambiamenti di trascrizione dei geni, sintesi proteica e regolazione epigenetica. La muscolatura scheletrica rappresenta oltre il 40% del peso della parte magra del corpo e il suo sviluppo è determinato dall'indice di sintesi e dalla degradazione proteica (Rehfeldt et al., 2004). Il tessuto adiposo subisce un processo di deposizione e riassorbimento costante durante tutta la vita dell'animale. La programmazione nutrizionale regola l'accrescimento di tali tessuti attivando o disattivando i geni. Queste alterazioni epigenetiche possono essere trasmesse da generazione a generazione. Le indagini attuali indicano che la proliferazione, la differenziazione e la morte cellulare programmata sono controllate da piccoli acidi ribonucleici denominati microRNA (Bengestrate et al., 2011). Comprendere i cambi dell'RNA messaggero ed i profili di microRNA dei suini alimentati con diete diverse, può rivelare i principali marcatori epigenetici che regolano gli accrescimenti dei suini. Le nuove tecniche, che includono l'analisi dell'espressione genica globale, potrebbero chiarire questi eventi critici, che probabilmente sono governati da alcuni RNAs chiave. Capire i meccanismi collaterali della regolazione mediata dai nutrienti sull'accrescimento di ossa, grasso e muscolo è condizione sine qua non per il miglioramento della produzione suinicola.
Cellule satelliti delle fibre muscolari
I muscoli contengono un gruppo di cellule precursore che si autorinnovano, che sono responsabili degli accrescimenti muscolari durante tutta la vita del suino. Queste cellule satellite rimangono nella parte esterna delle fibre muscolari e, in condizioni favorevoli, si moltiplicano e si differenziano in muscolo in crescita. Gli accrescimenti e la dimensione dei muscoli sono determinati dal numero (iperplasia) e dimensione (ipertrofia) delle fibre muscolari. L'accrescimento post-natale è un evento ipertrofico, dato che il numero delle fibre muscolari scheletriche si stabilisce al momento della nascita; tuttavia, i deficit nutrizionali prima dello svezzamento, possono interrompere l'allungamento dei miotubi esistenti, portando ad una riduzione del numero delle fibre muscolari (Rehfedlt et al., 2004). Anche lievi restrizioni (70%) di fosfato nella dieta hanno un impatto sulla moltiplicazione delle cellule satelliti e sull'attività dei suinetti appena nati (figura 1); a loro volta, i suinetti che ricevono una dieta con una quantità di fosfati al di sopra di quello richiesto non sono più efficienti nella conversione alimentare (Alexander et al., 2012). I geni che governano la moltiplicazione e differenziazione delle cellule satellite sono ottimi marcatori per determinare la complessa interazione tra i nutrienti e gli accrescimenti dei tessuti magri(carne) durante la vita produttiva del soggetto. Sono già stati identificati vari microRNAs come marcatori epigenetici e come regolatori della programmazione delle cellule satellite. Questo ed altri studi dimostrano la necessità e l'importanza della ricerca sulla nutrigenomica neonatale per l'industria suinicola.
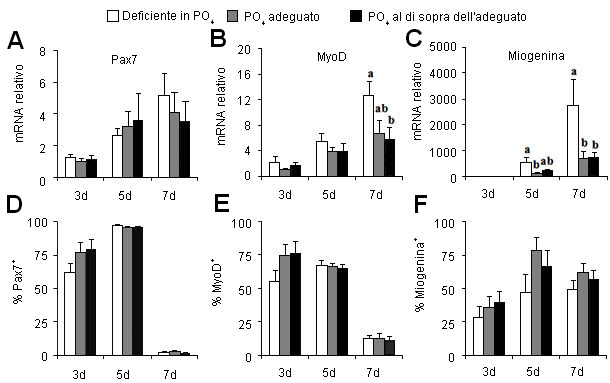
Figura 1. Effetto del fosfato contenuto nella dieta sui geni che regolano la moltiplicazione (Pax7) e la differenziazione (MyoD, Myogenin) delle cellule satellite. Espressione relativa dei geni (fila superiore) e proteina in vitro (fila inferiore) (Alexander et al., 2012).
Cellule madri mesenchimali (MSCs)
L'accrescimento post-svezzamento è anche parzialmente regolato da cellule madri mesenchimali (MSC). Una MSC possiede la capacità di autorinnovarsi e di essere multipotenziale. In condizioni favorevoli, le MSCs possono differenziarsi in ossa, cartilagine e tessuto adiposo, non solo, ma anche in cellule non mesodermiche come neuroni, epatociti, cellule di langerhans del pancreas e cellule endoteliali (Chen et al., 2004; Oswald et al., 2004; Pournasr et al., 2011; Tzeng et al., 2015). L'assegnazione di una certa linea cellulare di MSCs è strettamente regolata da segnali nutrizionali. La manipolazione dell'assegnazione delle linee delle MSCs mediante programmazione nutrizionale si è convertita in una strada innovativa e importante per promuovere gli accrescimenti durante tutta la vita del suino. La supplementazione della dieta si è dimostrata in grado di controllare le popolazioni e l'attività delle MSC. Per esempio: il diidrossicolecalciferolo [1,25(OH)2D3], un ormonte critico per lo sviluppo osseo e la produzione animale, stimola le MSCs suine alla differenziazione di una linea cellulare adiposa (Mahajan and Stahl, 2009) (figura 1). In modo del tutto similare, il livello di calcio della dieta anch'esso ha un grande effetto sull'attività e l'assegnazione delle linee di MSCs. Un eccesso di supplementazione aumenta significativamente la moltiplicazione delle MSC e determina la differenziazione adipogenica piuttosto che la osteogenica (Li and Stahl, 2014).
Questi studi indicano che la supplementazione neonatale con vitamine e minerali hanno un forte impatto sullo sviluppo osseo e sulla composizione corporale mediante la regolazione delle MSC e la programmazione delle cellule satelliti. In futuro, gli sforzi saranno concentrati sull'uso della nutrigenomica per identificare ed ottimizzare i componenti nutritivi per raggiungere una maggior produzione con la qualità della carne desiderata.
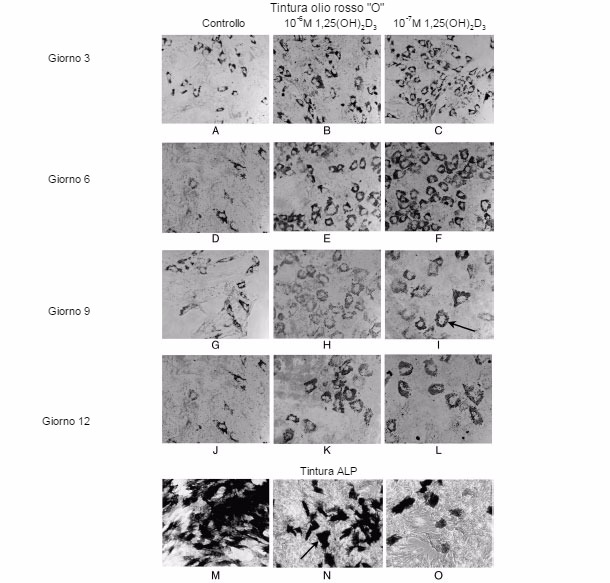

Figura 1. Tintura con olio rosso 'O' per lipidi neutri nelle cellule adipose e tintura di fosfatasi alcalina (ALP) delle cellule tipo osteoblasto (Mahajan and Stahl, 2009). L'idrossicolecalciferolo [1,25(OH)2D3] promuove l'adipogenesi delle cellule madri mesenchimali nei giorni 3 (A-C), 9 (G-I) e 12 (J-L) post-differenziazione. Tuttavia ha inibito la osteogenesi delle cellule madri mesenchimali (M-O).


