Il contatto progressivo con microbi ambientali durante i primi giorni di vita contribuisce alla colonizzazione del tratto gastrointestinale (GI) da parte di batteri e allo sviluppo di un equilibrio della flora GI. Questo permette lo sviluppo del tessuto linfoide associato alle mucose (MALT)che è in grado di produrre una risposta immunitaria attiva contro microbi patogeni ma che tollera gli antigeni non patognei come i batteri commensali.
Una buona performance nelle fasi iniziali della produzione si ottiene quando le condizioni ambientali non presentino una sfida alla barriera del tratto GI in modo che l'energia venga destinata alla crescita. Questo effetto veniva ottenuto ad un basso costo con l'uso degli antibiotici promotori di crescita, che inoltre riducevano la trasmissione di patogeni alla filiera alimentare. L'effetto degli antibiotici sulla flora GI dipende dal suo spettro d'azione, dosi, via di somministrazione e le caratteristiche farmacocinetiche-farmacodinamiche. Con differenti antibiotici si riesce ad ottenere un effetto promotore di crescita nel suinetto attraverso l'azione depressiva esercitata sui differenti batteri.
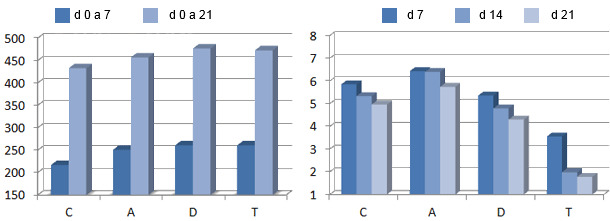
Nelle figure 1 e 2 possiamo vedere come antibiotici diversi migliorarono il consumo di mangimi in suinetti svezzati sani, ma hanno avuto differenti effetti sulla microflora intestinale (C = controllo, A = amossiicillina, D = doxiciclina, T = tilmicosina). Attraverso tecniche molecolari si è osservato che l'uso di questi antibiotici produce una riduzione della diversità della flora indipendentemente dal tipo di antibiotico.

 |
|
| Figura 1. Consumo di mangimi, gr/gg. | Figura 2. Conteggio degli enterobatteri, log10 CFU/g. |
Trevisi et al., 2011
Attualmente gli obiettivi della UE di produrre prodotti animali più sicuri includono la riduzione significativa del rischio che gli alimenti contengano patogeni enterici ed antibiotici. Inoltre, un minore utilizzo di antibiotici a fini terapeutici si considera necessario per ridurre la diffusione dell'antibioticoresistenza in medicina umana, e questo stimola la ricerca a trovare alternative pratiche all'uso degli antibiotici in alimentazione animale.
Il tipo di alimentazione, la scelta degli ingredienti e l'aggiunta di additivi possono modulare la microflora GI, riducendo il costo energetico del mantenimento e controllando pure i batteri patogeni. In seguito si riassumono alcuni strumenti pratici per aiutare a raggiungere questo obiettivo:
1- Formulazione basica. La qualità dei polissacaridi della dieta influenza la variabilità della microflora, ma deve essere sincronizzata con l'ingestione di proteina per minimizzare l'eliminazione di metaboliti della degradazione proteica. L'eccesso di alcuni nutrienti (zucchero, ferro, ecc…) può sovrastimolare i batteri patogeni e la migliore soluzione è apportare carboidrati altamente digeribili e poche ( ma buone) fonti proteiche.
2- Azione diretta sulla microflora GI: gli acidi organici sono i più affidabili, sopratutto se in combinazione e protetti. Da un altro lato, gli oli essenziali richiedono dosi elevate e vengono assorbiti troppo velocemente dal tratto digerente mentre il plasma rimane un'alternativa interessante ma costosa.
3- Potenziamento della barriera intestinale. L'ambiente materno è il principale fattore che contribuisce alla microflora GI dei suinetti neonati; la manipolazione della microflora GI della scrofa con la dieta (aggiungendo probiotici) ha un successo parziale nel modificare la microflora dei suinetti, la sopravivenza di questi e le performance della figliata prima e dopo lo svezzamento. Tuttavia, questa strategia non è ancora molto diffusa tra gli allevatori.
Durante lo svezzamento, l'apporto di microbi al mangime può contribuire a mantenere o ristabilire l'equlibrio a favore dei batteri commensali, che soffrono di anoressia temporale provocata dallo stress dello svezzamento. Pertanto dobbiamo disporre di probiotici specifici per i suini, come per esempio alcuni ceppi di Lactobacillus amylovorus.
Alcuni possibili probiotici sono stati studiati per contrastare patogeni enterici a partire dalle loro proprietà (produzione di molecole battericide, stimolazione della risposta immunitaria, concorrenza per i recettori o punti di incastro, ecc.). In genere i dati mostrano che la somministrazione orale può essere favorevole o almeno innocua. Indubbiamente ci sono casi in cui sono stati somministrati probiotici a suini durante un episodio infettivo e la risposta è stata negativa per la salute animale dato che differenti meccanismi di risposta immunitaria sono coinvolti. Le differenze nei risultati possono anche essere dovute ai diversi modelli applicati negli studi oppure ad ambienti GI già diversi in partenza.
Ci sono pochi dati affidabili sulle risposte immunitarie specifiche dei batteri commensali e sull'interazione tra batteri "selvaggi" con i probiotici somministrati oralmente. In contropartita i probiotici non sempre sono efficaci; il criterio di tolleranza è valido per soggetti sani ma hanno un certo rischio in soggetti esposti a patogeni. Altri probiotici come i lieviti ed alcuni dei loro sottoprodotti, sembrano essere promettenti per l'inclusione nei mangimi dei suinetti.
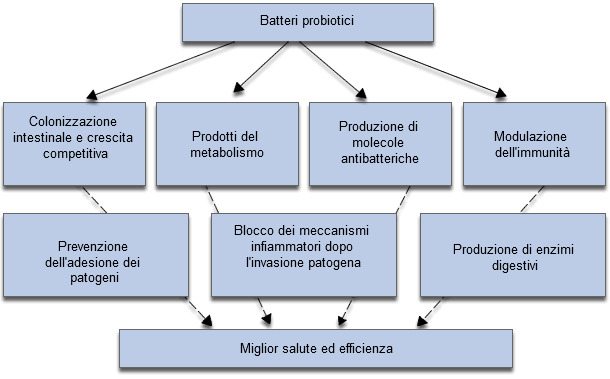
Figura 3- I meccanismi implicati sugli effetti positivi dei probiotici sull'accrescimento e la salute degli animali.
4- Usare aminoacidi. La supplementazione con triptofano e treonina può compensare l'aumento delle "spese" dovuto ad una infiammazione, e alla produzione di muco ed immunoglobuline; particolarmente in suini più sensibili alla colibacilosi. Ora esistono tests molecolari per l'identificazione della sensibilità individuale degli animali e questo può aiutare non solo la selezione genetica ma anche migliorare il management alimentare.
5- Ossido di zinco. A dosi terapeutiche altera significativamente la microflora e può migliorare la crescita ma non è sostenibile dal punto di vista ambientale.


