Le emissioni di ammoniaca (NH3) nel settore agricolo dell'Unione Europea (UE) nel 2020 sono state pari a 3,2 Mt, il 96,6% delle emissioni totali di questo gas, di cui si stima che il 67% sia dovuto alla gestione dei reflui zootecnici, con un leggero calo del 5% rispetto al 2008. Mentre le emissioni totali di gas a effetto serra (GHG) nell'UE sono diminuite del 27% nel periodo 2008-2020, quelle corrispondenti al settore agricolo sono rimaste pressoché immobili intorno a 465 Mt di CO2 eq/anno, 16,9 % delle emissioni totali nel 2020, di cui il metano (CH4) è responsabile per il 44,5%. È urgente ridurre queste emissioni per combattere il riscaldamento globale e i suoi effetti.
L'azoto totale e ammoniacale nei liquami è relativamente facile da misurare e quindi stimare il volume da applicare a un appezzamento in base alle esigenze della coltura e rispettare la Direttiva Nitrati. Al contrario, l'azoto, sotto forma di ammoniaca (NH3) o protossido di azoto (N2O) e il metano (CH4) non sono così facili da misurare, sono come nemici invisibili davanti ai nostri occhi.

Nemici perché sono gas che gli animali respirano e li colpisce mentre sono immagazzinate in fosse sotto i grigliati: perché con l'azoto volatilizzato diminuisce il valore fertilizzante ed economico del liquame; perché con le emissioni di CH4 si riduce la potenzialità di produrre biogas a fini energetici ed economici; o perché questi gas hanno effetti ambientali negativi, producono piogge acide nel caso di NH3 e ossidi di azoto, e hanno un effetto serra, circa 25 volte più della CO2 per CH4 e 298 volte più per N2O. Evitare le emissioni di NH3, N2O e CH4 deve far parte degli obiettivi di miglioramento della gestione dei reflui zootecnici.
Le reazioni più importanti che avvengono in una cisterna di liquami, o nella fossa sotto i grigliati, che influenzano le emissioni sono illustrate nella figura.
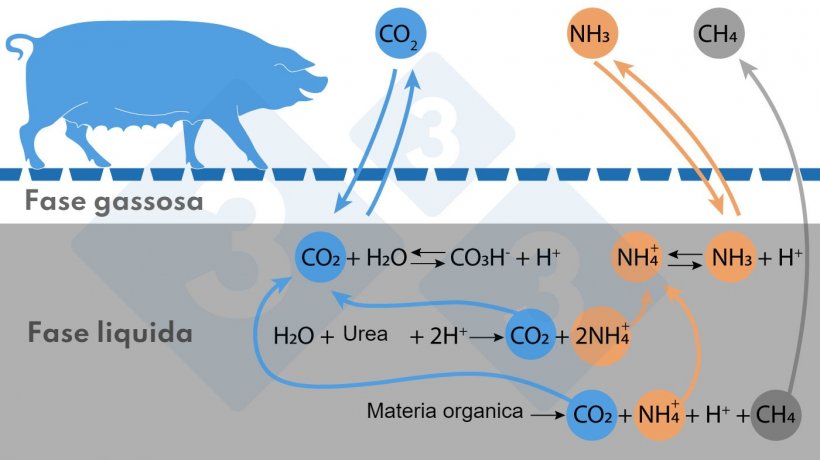
La principale fonte di azoto ammoniacale è l'urea, seguito dalla decomposizione anaerobica della materia organica con contenuto proteico. L'azoto ammoniacale si trova nel mezzo liquido in forma ionizzata (NH4+) e sotto forma di NH3. Il bilancio NH4++/NH3 dipende dal pH e dalla temperatura; all'aumentare della temperatura o del pH, l'equilibrio si sposta verso destra (come indicato nella figura), formando più NH3, che è volatile.
L'origine del CH4 è la decomposizione anaerobica della materia organica. Maggiore è la digeribilità dei solidi volatili (SV) contenuti nella materia organica nel liquame, maggiore è la quantità di CH4 che può essere prodotta.
Un terzo gas che viene emesso è il diossido di carbonio (CO2), che non è considerato un gas serra perché è di origine biogenica. Nel mezzo liquido, questo gas è in equilibrio con il bicarbonato (CO3H-), che permette di regolare il pH del mezzo. Quando i protoni (H+) coinvolti nelle reazioni indicate si accumulano, potrebbe abbassare il pH, ma in questo caso l'equilibrio CO2/CO3H- si sposta a sinistra e viene emessa CO2, contribuendo a mantenere il pH intorno alla neutralità o leggermente più alto. Ciò influisce negativamente sul consumo di acido se si desidera acidificare i liquami per evitare l'emissione di NH3.
Le emissioni dirette di N2O avvengono a seguito di reazioni di ossidazione dell'ammonio a nitriti o nitrati, o di riduzione di questi a gas N2. Queste reazioni possono avvenire in modo controllato in sistemi biologici NDN (nitrificazione - denitrificazione) o in modo incontrollato su superfici ruvide esposte all'atmosfera (vasche con crosta naturale, cumuli di frazione solida separata,...). Dell'NH3 che volatilizza si considera che l'1% si ossida a N2O in atmosfera (emissioni indirette).








