Per combattere un particolare problema clinico in una qualsiasi specie animale, è necessario stabilire una diagnosi accurata della malattia. In tutti i casi, l'esame clinico del paziente o dei pazienti è la pietra miliare per progredire nella diagnosi.
Le epidemie improvvise rappresentano sfide significative sia per gli allevatori sia per i veterinari, che devono individuare le cause del problema e intervenire per ripristinare la normalità. In queste circostanze, il veterinario suiatra diventa un investigatore, poiché deve valutare molteplici elementi che possono contribuire alla causa della malattia in uno scenario complesso in cui intervengono aspetti legati all'ambiente, all'alimentazione, alla biosicurezza, all'epidemiologia, alla presenza di molteplici patogeni e interazione uomo-suino...

Le malattie che colpiscono un gruppo di suini in un allevamento sono solitamente di origine infettiva o nutrizionale (tossicità o carenza). Il primo approccio diagnostico prevede sempre approfondite indagini cliniche ed epidemiologiche da parte del veterinario. Se l'esito clinico determinasse la mortalità o la grave compromissione dei suini, l'autopsia di alcuni di essi (quelli considerati rappresentativi della condizione) dovrebbe fornire alcuni indizi sulla causa o almeno consentire di escludere determinate eziologie.
La necroscopia deve essere svolta in modo ordinato, sistematico e completo.
Nella maggior parte dei casi la presenza di lesioni non fornisce cause specifiche, ma può aiutare a orientarsi su esse o a restringere l'elenco delle diagnosi differenziali.
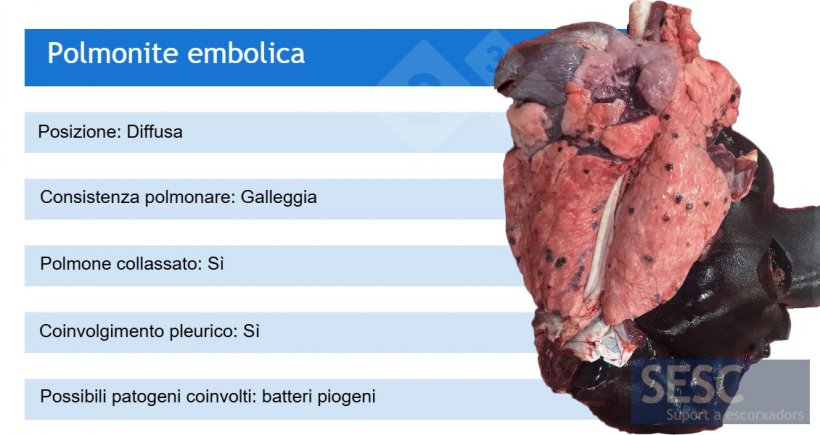
Ad esempio, i quadri macroscopici di polmonite offrono una serie di possibilità eziologiche, anche se in molti casi è necessario andare oltre e utilizzare test (di laboratorio) aggiuntivi.
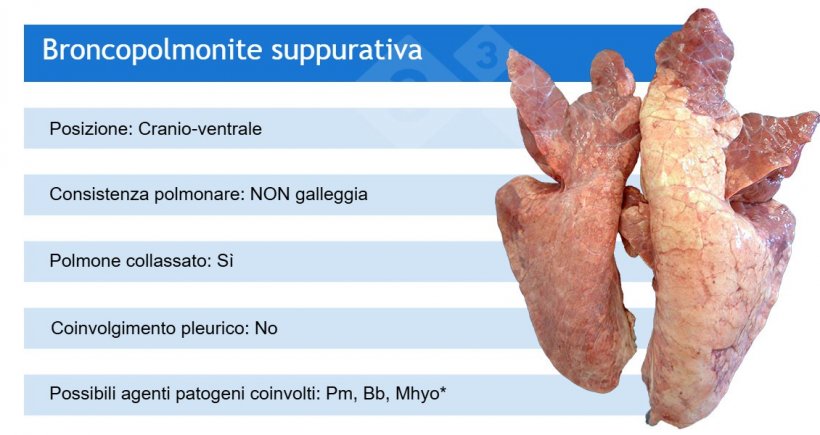
*Il Mhyo è spesso coinvolto nella broncopolmonite suppurativa in quanto agente patogeno scatenante (che causa per primo la polmonite broncointerstiziale).
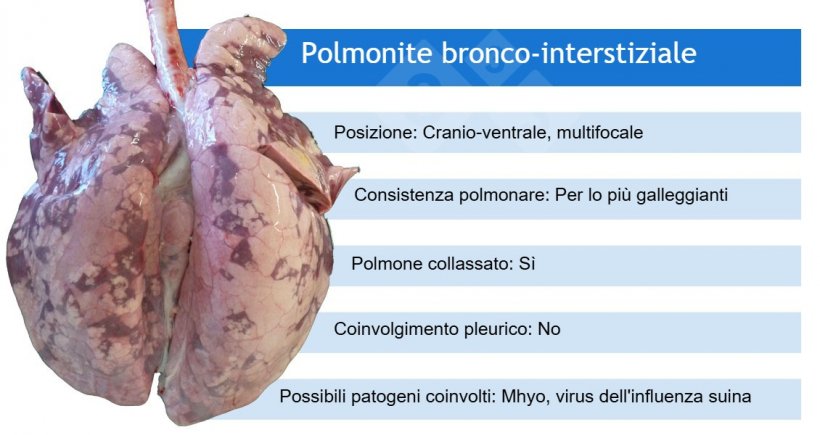
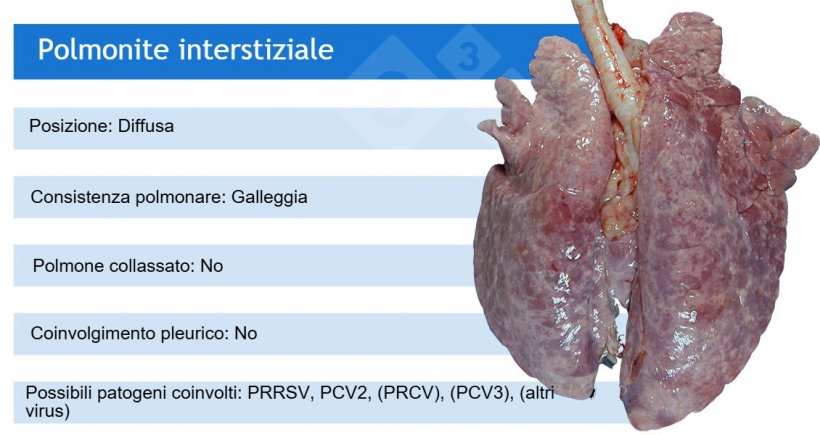
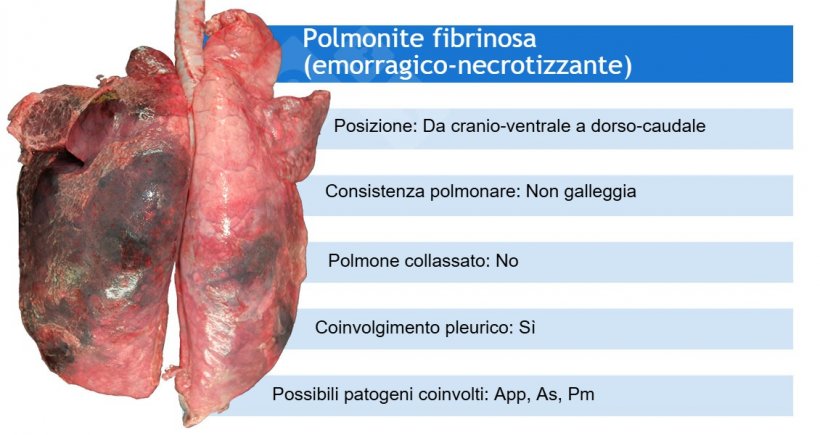
Analisi di laboratorio: non è tutto oro ciò che luccica!
Diversi approcci analitici aiutano a identificare possibili agenti patogeni (virus, batteri, parassiti, funghi) o tossine coinvolti in un problema clinico. I test più ampiamente utilizzati oggi sono i test di biologia molecolare, come la PCR (Polymerase Chain Reaction) e le sue varianti (qualitative, quantitative, per DNA o RNA). Il grande vantaggio di questa tecnica è la sua sensibilità (capacità di rilevare quantità minime di genoma patogeno o gene che codifica una tossina), ma ha anche un grande svantaggio, poiché: La semplice rilevazione di un agente patogeno o di una tossina in un contesto endemico non è sufficiente per stabilire una diagnosi eziologica inequivocabile.
Altre tecniche di laboratorio come l'isolamento batterico (incluso l'antibiogramma) sono molto utili, poiché permettono di stabilire una diagnosi eziologica e di indicare un possibile trattamento efficace. D'altra parte, le tecniche di rilevamento degli anticorpi sono ottimi strumenti di monitoraggio, ma offrono possibilità diagnostiche limitate, poiché la presenza di questi anticorpi dipende dallo stato vaccinale e/o infettivo, nonché dall'immunità materna.
Istopatologia: un valore aggiunto per confermare l'indagine diagnostica
Oltre ai test di laboratorio focalizzati specificamente sulla determinazione di agenti patogeni o tossine, l'istopatologia può fornire un solido quadro per stabilire la causa effettiva di un problema clinico.
Il rilevamento di un dato patogeno o tossina deve essere coerente con le osservazioni cliniche, epidemiologiche e la rilevazione delle lesioni macroscopiche, e l'analisi istopatologica può confermare definitivamente tale coerenza.
Un buon esempio dell'utilità della valutazione microscopica sarebbe il rilevamento di un virus tramite PCR in un problema respiratorio in cui le tipiche lesioni istologiche causate da questo agente non sono presenti nel polmone (supponendo che il suino o il gruppo di suini siano rappresentativi della malattia osservata). Uno scenario del genere dovrebbe indurre a riconsiderare la diagnosi sospetta e ad accertamenti più approfonditi.
Il veterinario suiatra dovrebbe considerare l'istopatologia uno strumento molto prezioso, almeno tanto importante quanto la PCR, l'isolamento batterico o la rilevazione degli anticorpi. L'analisi microscopica consente diagnosi morfologiche che confermano o contraddicono quanto stabilito attraverso risultati clinici, epidemiologici o di laboratorio, contribuendo così a stabilire la probabile eziopatogenesi del problema clinico. Queste informazioni generali sono importanti, poiché rappresentano una sorta di indicatore dell'efficacia o meno delle misure di controllo e prevenzione messe in atto per combattere la malattia.
Prelevare campioni per l'istopatologia (e altri esami di laboratorio) è relativamente facile, ma richiede una certa conoscenza della patogenesi della malattia, nonché alcune competenze tecniche:
- I campioni dovrebbero essere prelevati da carcasse fresche, idealmente da suini morti di recente o soppressi.
- I tessuti devono essere fissati immediatamente mediante immersione in formalina tamponata al 10%.
- Si sconsiglia di inviare campioni refrigerati per l'analisi istopatologica, poiché si verifica un certo grado di autolisi.
- Il congelamento dei campioni implica la presenza di molteplici artefatti che compromettono l'interpretazione microscopica.
- La dimensione del campione di tessuto deve essere relativamente piccola (o almeno sottile per favorirne la fissazione).
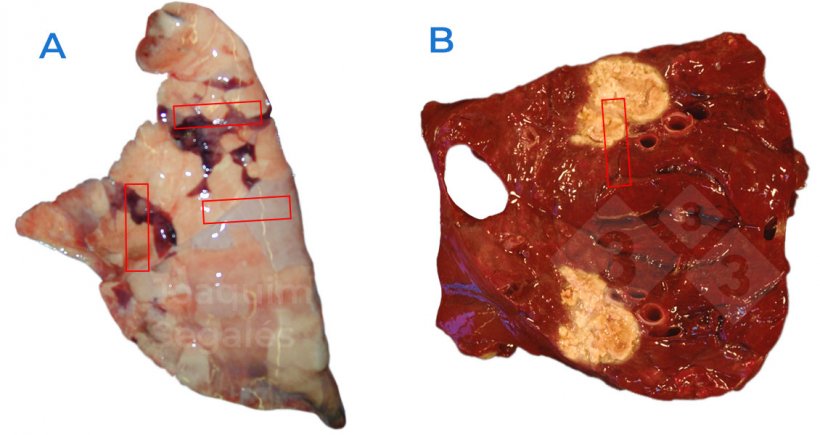
- Il campione dovrebbe includere sia le aree macroscopicamente interessate sia frammenti di tessuto presumibilmente normale (Figura 1).
- Nel caso di campioni intestinali, è importante aprire l'intestino longitudinalmente per garantire che la formalina entri in contatto diretto con la mucosa enterica.
- Al contrario, un organo di grandi dimensioni come il cervello è meglio venga fissato nella sua interezza o per metà, per garantire che la topografia del cervello venga mantenuta durante la fissazione; in seguito, il patologo può selezionare la parte appropriata per cercare di stabilire la diagnosi più probabile.
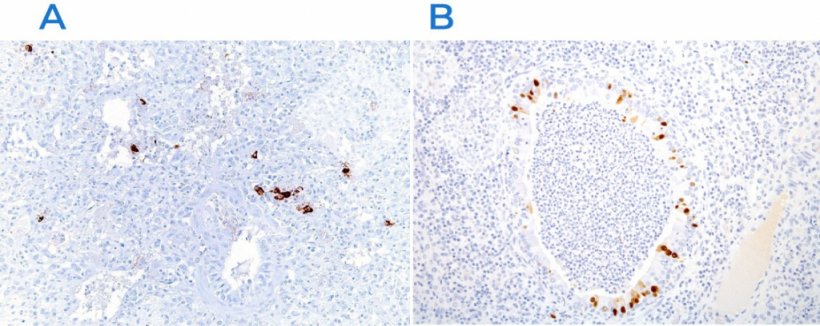
È importante notare che, oltre alla semplice analisi istopatologica (basata sulla colorazione con ematossilina-eosina, Figura 2), altri test patologici aggiuntivi possono aiutare nella ricerca degli agenti eziologici.

I più usati sono l'immunoistochimica (Figura 3) e l'ibridazione in situ (Figura 4), che consentono di rilevare i patogeni nel sito d'azione, supportandone il ruolo nel contesto clinico e patologico. Esistono inoltre altre tecniche (colorazioni istochimiche) che non sono sufficienti per stabilire un'eziologia specifica, ma possono fornire indizi sulla causa (ad esempio, la colorazione di Groccot per rilevare funghi o la colorazione di Gram per rilevare batteri gram-positivi o negativi).

In sintesi, il veterinario suiatra, oltre alle proprie indagini cliniche, epidemiologiche e delle lesioni macroscopiche, dispone di diverse possibilità analitiche, nelle quali l'istopatologia può svolgere un ruolo fondamentale. Una comunicazione efficace tra medici e patologi migliora le capacità diagnostiche, portando ad una risoluzione più tempestiva ed efficace dei problemi clinici.




