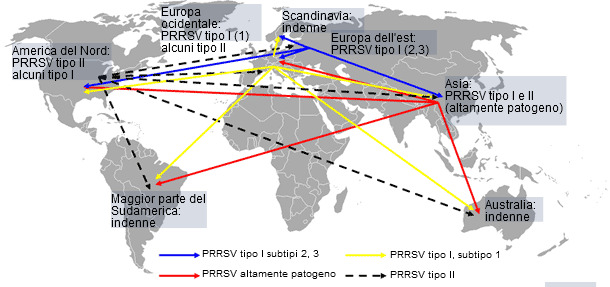
In un recente studio eseguito dall'Università di Iowa si è rilevato che la sindrome respiratoria e riproduttiva suina (PRRS) continua a causare grandi perdite economiche agli allevatori. I ricercatori hanno stimato che il costo negli USA della PRRS può raggiungere i $664 milioni annuali ovvero $1,8 milioni al giorno(Holtkamp D, et al. 2011). Altri rapporti suggeriscono che l'impatto in Canada, Messico, Asia ed Europa sia di uguale entità. Dall'inizio della malattia, oltre 20 anni fa, i tipi I e II del virus PRRS si sono diffusi geograficamente, guadagnando diversità genetica e probabilmente, aumentando la virulenza (Murtaugh MP, et al. 2010; Li B, et al. 2006). Nell'Europa occidentale, senza dubbio, l'impatto economico della PRRS tuttavia è dibattuta in molti studi controversi, che spaziano da episodi molto gravi a casi subclinici. La minor gravità della malattia in Europa può essere dovuta ad una relativa elevata prevalenza, con molti siti a ciclo chiuso e alla predominanza del virus tipo I, che nonostante presenti una ampia gamma di ceppi genetici (Stadejek T, et al. 2008), inducono a segni clinici respiratori meno gravi rispetto al virus tipo II (Martinez-Lobo FJ, et al. 2011). Indipendentemente da questa interessante discussione, il rischio di introduzione di nuovi ceppi di PRRSV, tipo I o II, in zone ad alta densità suinicola con predominanza di cicli chiusi nell'Europa occidentale è sempre presente. Inoltre il rischio di trasmissione intercontinentale degli isolati ad alta patogenicità di virus PRRS identificati in Asia è reale. Allo stesso tempo in altre parti del mondo come Australia, la maggior parte del Sudamerica e Scandinavia, l'introduzione di qualsiasi virus PRRS potrebbe essere catastrofica per l'industria locale.(figura 1). Questa situazione globale indica che il virus PRRS di per sè è un rischio potenziale per le possibili conseguenze di trasmissione tra regioni e pertanto non deve essere sottovalutato.
Figura 1. Distribuzione globale del virus PRRS ed ipotetica trasmissione intercontinentale

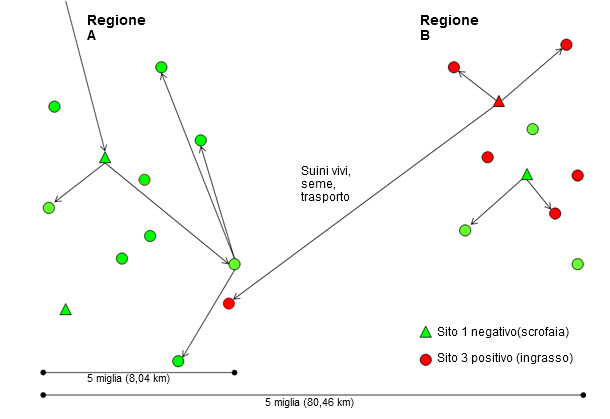
Senza una metodica valida per raggruppare gli isolamenti virali di PRRSV e per le finalità di questo articolo, si considererà come isolamento "nuovo", il ceppo eterologo per almeno il 3% della sequenza su ORF 5 rispetto a qualsiasi altro virus isolato in un sistema, oppure all'interno di un gruppo di allevamenti negli ultimi 3 anni. L'isolamento di un virus "residente" sarà giusto il contrario. In molti casi questa soglia arbitrale può non aver nessun significato e sarà utilizzato solamente come valore di riferimento. La rapida diffusione del virus PRRS a lunghe distanze lungo gli anni 90 , ed il relativo confinamento geografico degli isolati residenti negli ultimi anni, quando sono stati utilizzati protocolli di monitoraggio più sensibili, suggeriscono che i nuovi virus hanno bisogno di suini vivi, seme o veicoli contaminati per effettuare la trasmissione tra regioni (figura 2). Come ipotesi, i nuovi isolati di virus PRRS si creano a partire dai continui cambi del virus all'interno delle regioni dove è presente la trasmissione continua all'interno e tra allevamenti (regione B nella figura 2). Nei paesi dove si pretende di mantenere gli allevamenti di moltiplicazione ed i centri di inseminazione PPRSV negativi, dove sono stati raggiunti importanti progressi, nei protocolli di quarantena e di distribuzione di materiale seminale, la causa più frequente di trasmissione a lunga distanza è la movimentazione di suini svezzati, la movimentazione di grassi positivi al virus e l'uso di mezzi di trasporto contaminati (regione A, figura 2). Per disgrazia, la distribuzione della rimonta e di seme positivi al virus è ancora una realtà in molti paesi. Considerare una regione, o sistema produttivo, o allevamento, che per il fatto di essere positivo ad un ceppo di virus PRRS, possa accettare seme infetto o rimonta infetta è molto pericoloso, dato che si potrebbe introdurre un ceppo più virulento.
Figura 2. Introduzione di un nuovo isolato di virus PRRS dalla regione B alla regione A
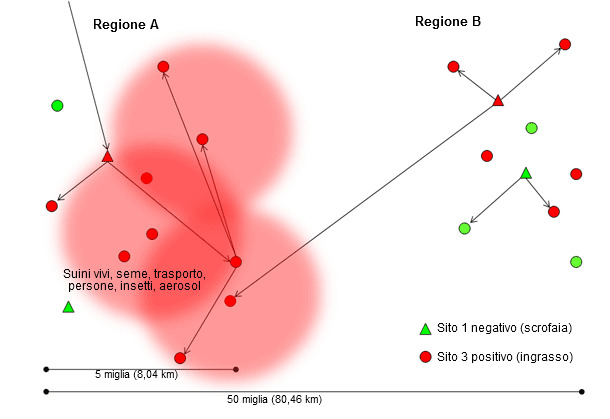
La ricerca portata a termine dal Dr. Scott Dee e Satoshi Otake dimostra che il virus PRRS può essere trasmesso tra allevamenti attraverso i mezzi di trasporto (Dee SA, et al. 2004), fomiti (Otake S, et al. 2002), persone (Otake S, et al. 2002), insetti (Otake S, et al. 2004), liquami ed aerosol (Dee SA, et al. 2005). La trasmissione per via indiretta è probabile che accada in distanze relativamente corte, dal primo allevamento infetto con un nuovo ceppo (figura 2), in aree ad elevata densità suinicola e che probabilmente si vede aggravata da misure insufficienti di biosicurezza. Normalmente quando il primo allevamento si vede infetto, altri allevamenti riceveranno suini con infezione acuta convertendosi in amplificatori del ceppo originario (regione A , figura 3). In questa situazione non si può fare gran che per contenere o ridurre l'epidemia. Curiosamente, tra i vari ceppi distinti che sono identificati in zone di elevata densità suinicola ad ogni anno, solamente alcuni ceppi sono capaci di passare ad altri allevamenti e tuttavia sono meno capaci di disseminarsi ampliamente e dominare una intera regione o sistema produttivo. I fattori che determinano quali ceppi di virus PRRS si diffondono e persistono in determinate aree geografiche, o flussi di animali, devono essere approfonditi; senza dubbio, si può ipottizzare che questi ceppi abbiano una capacità intrinseca di replicarsi molto efficace nei suini, di trasmettersi attraverso vie diverse , inclusa la via aerea , e l'esistenza di popolazioni di suini che mantengano l'infezione nel tempo e dissemini quantità significative di virus durante un periodo prolungato.
Figura 3. Disseminazione di un nuovo isolato di virus PRRS attraverso la regione A
Studi di controllo indicano che quando suini sensibili sono esposti a virus PRRS selvaggi possono eliminarlo per 70 - 100 giorni (Cano JP, et al. 2007; Linhares D, et al. 2012). Grandi popolazioni di suini negativi servono come amplificatori del virus nella regione appena infettata e rappresentano un enorme rischio per gli allevamenti vicini per un lungo periodo. Gli stessi studi rivelano che l'uso di vaccini vivi modificati in queste popolazioni recentemente infettate riducono la durata dell'eliminazione di circa 30 giorni. Si spera inoltre che le popolazioni che abbiano sviluppato immunità contro il virus vivo PRRS eliminino il virus eterologo (di recente introduzione) in minori quantità e durante meno tempo rispetto alla prima volta alla quale furono esposti o rispetto a popolazioni completamente sensibili. Ricordare che i suini negativi in fase di accrescimento amplificano i nuovi ceppi; il serbatoio dei ceppi isolati normalmente è l'ingrasso a flusso continuo o allevamenti a ciclo chiuso. Se i grassi sono allevati in un sistema tutto pieno tutto vuoto a livello d'allevamento, probabilmente un ceppo nuovo si elimina dopo l'uscita totale degli animali. I risultati osservati nei piani regionali di controllo della PRRS negli USA suggeriscono che il principio dell'uniformizzazione dell'immunità all'esposizione, che viene applicata con esito positivo a livello di scrofaia per il controllo del virus PRRS può rappresentare un'alternativa possibile per il controllo regionale.
Riassumendo, il destino che la PRRS impone ad una regione o regioni o filiere potrebbe essere superato con una miglior conoscenza dell'epidemiologia del virus e con la combinazione di strategie che hanno come obiettivo:
- Prevenire nuove introduzioni di virus attraverso l'applicazione sistematica di un programma di biosicurezza completo.
- Ridurre la fonte di nuovi ceppi cercando di eliminare il virus nelle popolazioni e dei flussi continui di animali endemicamente infetti.
- Contenere la diffusione di nuovi ceppi massimizzando l'immunità dell'allevamento, la biosicurezza e mettendo in pratica un sistema di vigilanza integrato per realizzare la tracciabilità del virus.
- Minimizzare l'impatto economico della malattia cercando di controllare l'esposizione e l'immunità attraverso l'utilizzo di filtri d'aria, biosicurezza, vaccinazione e cambiamento/miglioramento del flusso degli animali.