Una lunga carriera professionale nella ricerca sul PRRSV
Il Dr. Hans Nauwynck, Professore all'Università di Ghent (Belgio) ha una carriera di ricerca impressionante e produttiva. È autore di oltre 450 articoli peer-reviewed, 3 capitoli di libri e 76 tesi negli ultimi 30 anni. È considerato uno dei più importanti ricercatori europei, senza dubbio il più energico!... In questo articolo riassumiamo le nostre conversazioni su come il PRRSV si è evoluto sul campo nel tempo...

Problemi correlati con il PRRSV Tipo 1
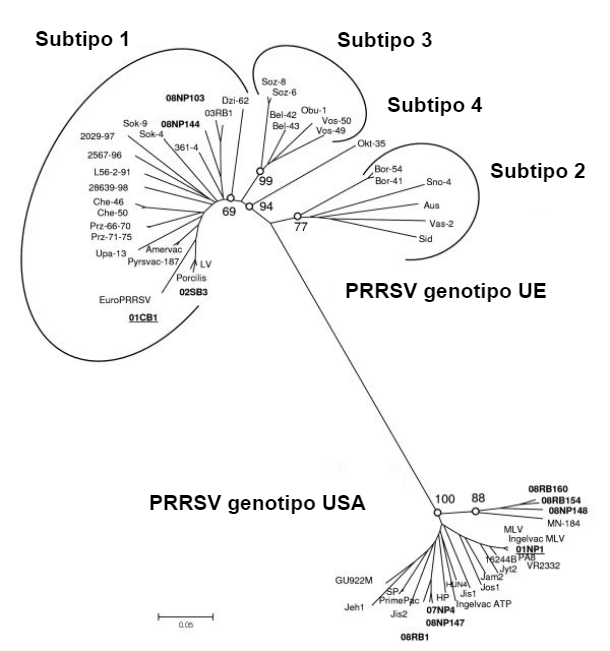
All'inizio della sua carriera (anni '90), ha condotto esperimenti per esaminare il comportamento dei ceppi PRRSV-1 e PRRSV-2. Sebbene entrambi inducessero insufficienza riproduttiva nelle scrofe, erano completamente diversi a livello delle vie respiratorie nei suini giovani: la difficoltà respiratoria era evidente con il tipo 2. I ceppi di tipo 1 hanno causato principalmente infezioni subcliniche. In quegli anni ha imparato che nell'UE si trattava di un virus completamente diverso da quello degli Stati Uniti / Canada. La grande distanza genetica era coerente con i risultati clinici (immagine 1). Anche le esperienze sul campo sono state molto diverse. Con i ceppi PRRSV-1, il virus si stava diffondendo molto lentamente negli ingrassi. Il virus ha impiegato l'intero ciclo di ingrasso per infettare tutti i suini. Ciò indicava una potenza di trasmissione molto inefficiente. Con il PRRSV-2 è stata riscontrata una diffusione più rapida. Negli Stati Uniti, gli scienziati hanno dimostrato una diffusione aerea. Negli anni 2000, in Russia / Bielorussia (sottotipi 2 e 3) sono stati identificati ceppi di tipo PRRSV-1 geneticamente remoti che erano molto più virulenti e patogeni. Più recentemente, il sottotipo 1 del PRRSV-1 si sta diffondendo più rapidamente e sta persino causando più malattie del solito (ceppi italiani)...
“L'Europa occidentale, non deve preoccuparsi del PRRSV di tipo 1 come agente patogeno responsabile dei problemi respiratori; dovrebbero temere e prestare attenzione alle malattie o co-infezioni associate ", dice il dottor Nauwynck. Ha creato un nome per i problemi respiratori legati alla PRRS nell'UE, "PRRS PLUS" (ha lanciato questo termine per i veterinari suini da campo.) Le molteplici co-infezioni da PRRSV con altri diversi patogeni rendono il PRRSV uno dei patogeni più importanti nell'UE. Di conseguenza, è essenziale disporre di un'analisi diagnostica completa. Tutti i patogeni devono essere identificati. In questo contesto, sono necessarie nuove diagnosi. Una conoscenza approfondita dei patogeni circolanti è essenziale per capire cosa sta succedendo in allevamento e per controllare il PRRS PLUS. Come dice lui: "Se i veterinari si prendono cura di tutte le possibili co-infezioni, i segni clinici respiratori della PRRS sostanzialmente scompaiono". Ritiene che gli allevamenti europei positivi possano allevare suini in modo molto efficiente quando controllano i cofattori e non hanno bisogno di eradicare il virus. Questo può cambiare, ovviamente, qualora la virulenza / patogenicità del virus aumenti in futuro...
L'evoluzione del virus può essere spiegata da una migliore comprensione delle interazioni virus-ospite: il ruolo dei recettori Siglec
Il suo team si è rivolto allo studio dell'interazione virus-ospite a livello molecolare e, di conseguenza, sono stati in grado di capire come il virus è cambiato nel tempo, in particolare come è aumentata la sua potenza di trasmissione, come descritto sopra, e la sua patogenicità .
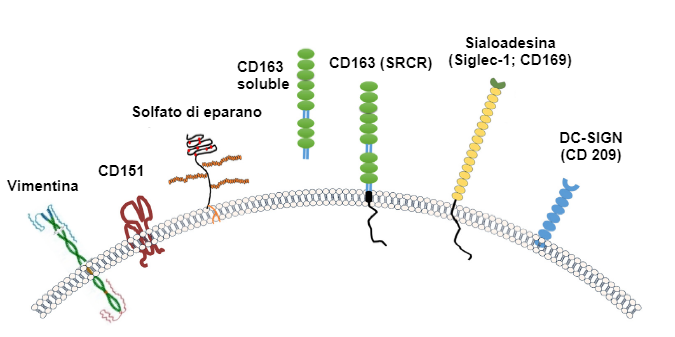
La sua equipe ha dimostrato che l'ingresso del virus nei macrofagi comporta più passaggi. Inizia con l'interazione del virus con i recettori Siglec e continua dopo l'internalizzazione con l'interazione con il recettore CD163, che porta allo smontaggio del virus. Il PRRSV può utilizzare diversi Siglec ed evolversi nel tempo.
Siglec-10 può essere ipotizzato come il "recettore arcaico". Siglec 10 è presente in un piccolo gruppo di macrofagi nelle tonsille e in altri tessuti linfoidi ed è molto efficiente nel processo di ingresso del virus, dimostrando la sua lunga coevoluzione con il PRRSV. Questo Siglec è stato probabilmente utilizzato dal virus all'inizio della sua comparsa. A quel tempo, il PRRSV si stava replicando solo in questa piccola popolazione di macrofagi e probabilmente non stava causando segni clinici. Poiché siglec-10 è presente anche sui linfociti B, è stato in grado di legarsi ed entrare in queste cellule, ma senza infettarle. Questa potrebbe essere la base per la persistenza del virus nel suo ospite (serbatoio). Alla fine degli anni '80, il PRRSV probabilmente si è ulteriormente trasformato nel recettore Siglec-1 (= sialoadesina, CD169). Le cellule Siglec-1 positive sono presenti nei polmoni, nella placenta e nei tessuti linfoidi. La replicazione nei polmoni e nella placenta ha provocato problemi respiratori e riproduttivi. Questa era la base del nome PRRSV. Nel 2000, il virus nell'Europa occidentale ha iniziato a replicarsi nei macrofagi nasali, portando ad una maggiore trasmissione tra i suini. Il recettore responsabile di questo adattamento è sconosciuto; è diverso da Siglec-1 e Siglec-10. Il ceppo altamente virulento di Lena (PRRSV-1 sottotipo 3) sta causando patologia dei vasi, che è associata alla replicazione del PRRSV nei macrofagi venosi. Anche il recettore in questo sottogruppo di macrofagi è diverso da Siglec-1 e Siglec-10. I recettori nei macrofagi venosi e nasali sono in fase di studio.
Crede che il virus continui ad evolversi in forme che infettano sempre più sottopopolazioni di macrofagi.