Descrizione del Senecavirus A
Il Senecavirus A (SVA, anticamente conosciuto come il virus Seneca Valley) è un virus RNA non-enveloped di 30 nm. E' l'unico membro del genere Senecavirus, che appartiene alla famiglia dei Picornaviridae.

Comportamento del SVA e implicazioni patologiche
Il SVA è stato isolato nei suini nel 1988 ed è stato descritto come tipo-picornavirus fino al 2002, quando è stato isolato da una coltura cellulare contaminata e fu chiamato virus Seneca Valley (Reddy, Burroughs et al. 2007). Di fatto, il SVA è stato identificato come un virus non patogeno nell'uomo con proprietà oncolitiche e si sta valutando la sua efficacia come terapia contro il cancro in sperimentazioni cliniche nell'uomo (Rudin, Poirier et al. 2011). Il genoma completo è stato sequenziato nel 2008 (Hales, Knowles et al. 2008).
Le ricerche di campo in veterinaria suggeriscono che il SVA circola tra gli animali domestici, almeno fin dagli anni '80. Sono stati rilevati anticorpi nei confronti del SVA nei bovini, ratti e suini (Knowles, Hales et al. 2006). E' stato anche proposto come agente causale della malattia vescicolare idiopatica (IVD) nei suini (Singh, Corner et al. 2012, Leme, Zotti et al. 2015). Riassumendo, l'Organizzazione Mondiale della Sanità (OIE), e la maggior parte dei paesi, considerano la dichiarazione obbligatoria di queste 4 malattie vescicolari dei suini: l'afta epizzotica(Aphtovirus), la malattia vescicolare suina (Enterovirus), la stomatite vescicolare (Rhabdovirus) e l'esantema vescicolare suino(Calicivirus). I casi di malattie vescicolari negativi a questi 4 virus si considerano "malattia vescicolare idiopatica".
Nonostante vari tentativi, non si è riusciti a riprodurre sperimentalmente la malattia vescicolare a partire dal SVA. Tuttavia, il virus è stato dimostrato mediante ibridazione in situ nelle lesioni vescicolari degli animali colpiti (figura 1). Attualmente si sta conducendo uno studio per tentare di riprodurre la malattia vescicolare con un SVA recentemente isolato nel Midwestern USA, proveniente da suini con malattia vescicolare idiopatica.
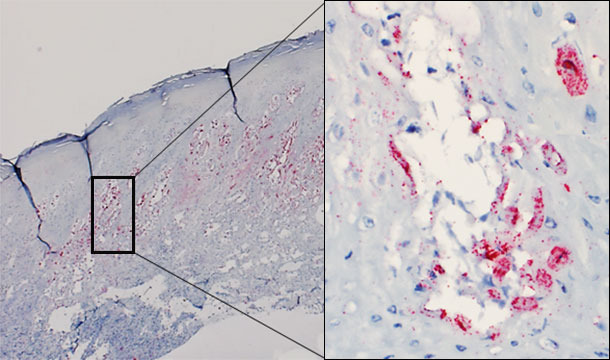
Figura 1 – Biopsia cutanea di una vescicola di un suino colpito. Si rileva la presenza del virus predominante nello strato spinoso dell'epidermide. Vesicola intraepidermica: virus che si replica nei cheratinociti.
Associazione con ETNL, in Brasile ed in USA.
Recentemente (Luglio 2015) il Brasile ha informato di una nuova sindrome associata al SVA. Il Dr. Vannucci, assieme ad altri 8 colleghi, hanno descritto una sindrome con perdite neonatali che colpisce i suinetti tra 0-7 gg di vita. La % di mortalità è molto elevata (40-80%) nei suinetti di 0-3 gg e minore (20-40%) in quelli di 4-7 gg. Le figliate di più di 1 settimana non sembrano essere clinicamente colpite. Una volta stabilita la malattia, inizia abbastanza rapidamente, una sindrome di deperimento che porta alla morte. La % di mortalità normale si ristabilisce in 4-10gg. Occorre rilevare che la maggior parte dei suinetti (>80%) hanno lo stomaco pieno di latte/colostro. A causa di queste caratteristiche abbiamo proposto il nome di mortalità neonatale epidemica transitoria (ETNL,epidemic transient neonatal mortality in sigla inglese)(Vannucci, Linhares et al. 2015)(figura 2).


Figura 2 - Caratteristiche acute e transitorie della mortalità neonatale epidemica transitoria (ETNL). A sinistra: aspetto tipico di una figliata colpita durante un focolaio di ETNL. Destra: una nuova figliata nella stessa sala parto di 10gg dopo l'episodio di mortalità.
L'esame patologico dei suinetti colpiti di vari allevamenti del Brasile e successivamente nel medio-ovest degli USA, non rilevarono lesioni macroscopiche o istopatologiche comuni/consistenti che potessero spiegare la causa della mortalità. Un risultato consistente negli allevamenti con ETNL fu il rilevamento di grandi quantità di Senecavirus A in molti tessuti dei suinetti, incluso il cervello, sangue e tessuti linfoidi, il che indica una infezione generalizzata (Linhares, Rademacher et al. 2015) (figura 3). Non si trovò SVA nei tessuti dei suinetti non colpiti.
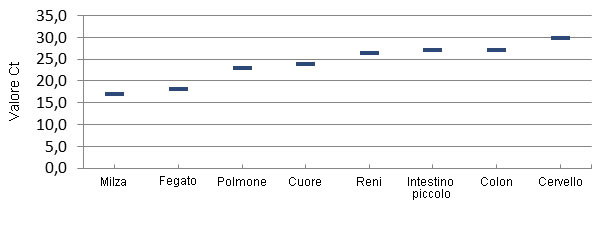
Figura 3 – Distribuzione del virus con PCR quantitativa nei tessuti di suinetti colpiti da ETNL.
Assieme alla sindrome ETNL, in alcuni allevamenti si riscontrarono casi di malattia vescicolare idiopatica con lesioni moderate o lievi al naso e/o zoccoli (bande alla corona, area interdigitale o cuscinetti plantari (figura 4). In altri allevamenti non furono descritte lesioni di tipo vescicolare, suggerendo che il SVA necessiti di altri fattori che contribuiscano a instaurare la malattia (presupponendo che il SVA causi la malattia). La IVD che accompagnava l'ETNL anch'essa presentava una natura transitoria, con lesioni che nel muso si curavano in alcuni giorni e quella degli unghielli in una o due settimane.
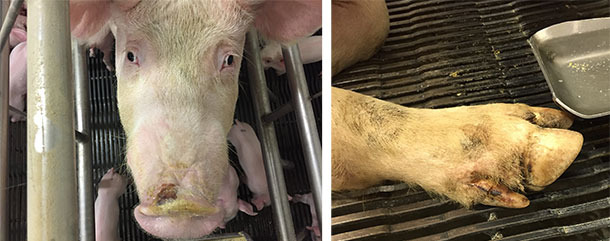
Figura 4. Lesioni al muso ed agli unghielli nei casi di malattia vescicolare idiopatica.
Importanza epidemiologica ed implicazioni
L'ETNL si diffuse molto rapidamente in Brasile, con episodi raggruppati nel tempo e nello spazio. In altre parole, quando si descriveva la sindrome in un certo allevamento, era molto probabile che gli allevamenti vicini la subissero anch'essi, indipendentemente dal sistema di produzione, dal flusso dei suini/persone o dalla fonte genetica o di mangimi. Ci sono stati esempi in Brasile e negli USA di allevamenti chiusi durante > 6 mesi (che non introducevano nè scrofe da riproduzione nè verri esterni) che ebbero la ETNL. In pratica, queste osservazioni suggeriscono che ETNL e/o IVD anch'esse si trasmettono per vie indirette.
Fino a questo momento, i primi allevamenti che hanno informato degli episodi (settembre 2014) non hanno avuto altri episodi ( che noi sappiamo). In altre parole, pare che l'ETNL fu un "episodio unico", per lo meno dopo di 1 anno. Considerando che la maggior parte degli allevamenti ha una % di rimonta del ~45%, ogni ~2 anni la maggior parte delle scrofe sono state sostituite e pertanto il rapporto tra soggetti sensibili : immuni/resistenti può cambiare significativamente. Questo può causare ondate di casi di ETNL ogni 1,5 a 2,0 anni.
Supponendo che tanto ETNL come IVD siano causati da SVA, questo virus ha una elevata % di trasmissione (a livello regionale e di allevamento), è molto immunogeno e genera una immunità di lunga durata(almeno 1 anno).
Uno studio recente di epidemiologia molecolare (Jianqiang et al. ASM science, Vannucci, Linhares et al 2015) mostró che ceppi contemporanei di SVA (USA e Brasile, di casi di ETNL e/o IVD) raggruppati separatamente dalla maggior parte dei ceppi storici isolati di SVA, suggerisce che SVA potrebbe essere cambiato recentemente ed aver aumentato la propria patogenicità. Altra possibilità è che il recente incremento di casi clinici associati con SVA potrebbe essere dovuto a variazioni (aumento) nella % di trasmissione e/o sopravvivenza ambientale del SVA.
Tuttavia dobbiamo ancora comprendere come e dove si "nasconde" lo SVA tra episodi e come si trasmette tra allevamenti. In altre parole, può lo SVA permanere infettante su alcuni ingredienti del mangime? Può essere trasportato dall'aria? Da vettori? Servono ulteriori studi per rispondere a queste domande.
Ulteriori studi in atto
Si stanno conducendo vari lavori di ricerca per chiarire temi come a) sviluppare / convalidare un ELISA per SVA, b) confermare il ruolo di SVA in ETNL/IVD, c) comprendere l'epidemiologia molecolare di SVA in Brasile e negli USA, d) protocolli di disinfezione nei confronti di SVA.
Si devono realizzare ricerche nei confronti delle malattie esotiche in ogni caso rilevato di IVD per scartare le altre 4 malattie vescicolari (includendo l'afta epizootica).
Ringraziamenti
Al Dr. David Barcellos, dell'Università Statale dell'Iowa ed all'equipe di ricerca dell'Università del Minesota.


