Introduzione
Si tratta di un allevamento commerciale a ciclo chiuso in Irlanda che passò da 600 a 1000 scrofe in un anno.

Il protocollo vaccinale usato era questo della tabella 1.
Tabella 1. Programma di vaccinazione.
| Vaccino | Scrofette | Scrofe | Verri | Suinetti |
| Parvovirus | Iniezione di 2 ml alla selezione | Iniezione di 2 ml 2 settimane prima del parto | Iniezioni di 2 ml due volte/anno | |
| Mal Rosso | Iniezione di 2 ml alla selezione e 2 settimane prima della copertura | Iniezione di 2 ml 2 settiman dopo il parto | Iniezione di 2 ml due volte/anno | |
| Colibacilosi e Clostridiosi | Iniezione di 2 ml 6 e 2 settimane prima del parto | Iniezione di 2 ml 2 settimane prima del parto | ||
| PRRS (vivo attenuato o MLV) | Iniezione di 2 ml alla selezione e a 60 gg post-copertura | Iniezione di 2 ml 6 gg dopo il parto e a 60 gg post-copertura | Iniezione di 2 ml due volte/anno | |
| PCV-2 | Iniezione di 1 ml allo svezzamento | |||
| Polmonite Enzootica | 1 ml a 10 - 14 gg dopo lo svezzamento |
Le scrofette sono di autorimonta. I verri si utilizzano solo per fare la ricerca calori. Le scrofette e le scrofe vengono coperte in inseminazione artificiale con seme da un unico fornitore.
L'allevamento più vicino dista 2 km.
Storico
L'allevatore ha contattato il veterinario in seguito ad un aumento di problemi respiratori, perdite di condizione corporale e aumento della mortalità in svezzamento ed ingrasso.
Indagine
Indagine Clinica
Durante una visita all'allevamento nel settembre 2017, si osservarono molti suinetti da 6 a 15 settimane di età con sintomi clinici di perdita di condizione corporale e respirazione addominale (figure 1 e 2). Rari colpi di tosse. La densità dei box era eccessiva.


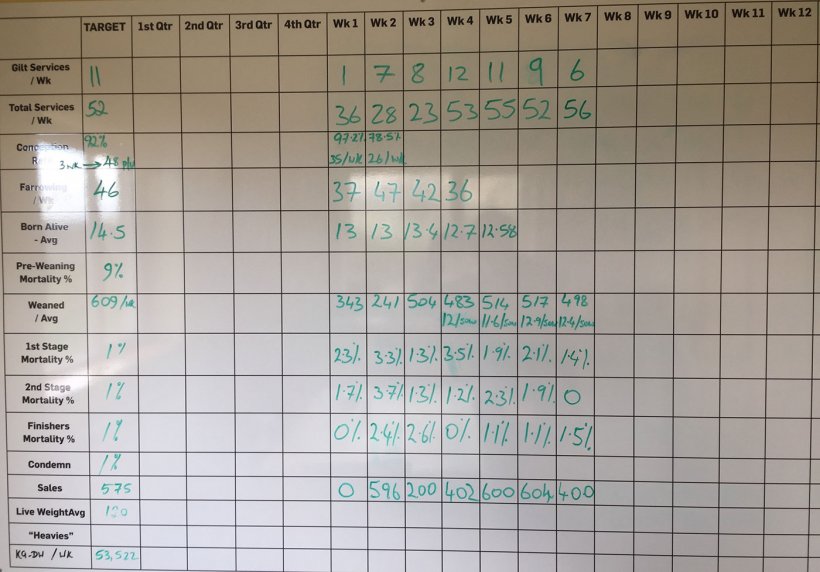
L'allevatore commentò che la mortalità tra svezzamento ed ingrasso era del 3,5 – 5%. Però quello che si vedeva nel tabellone era totalmente diverso (figura 3).
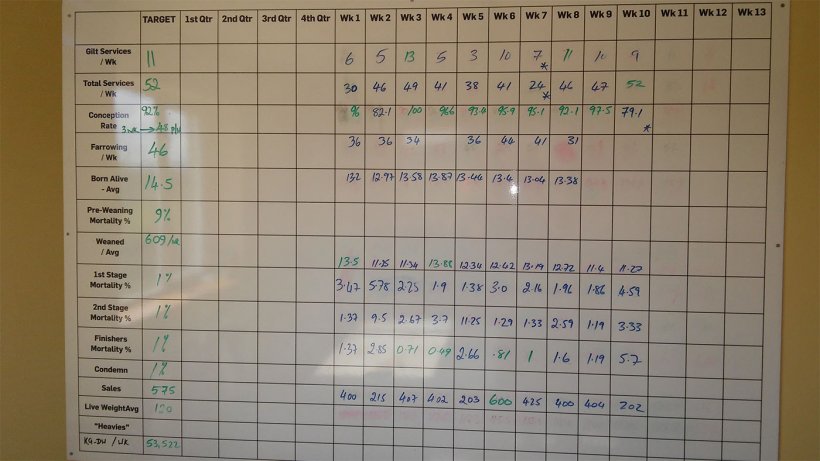
Secondo il tabellone la mortalità in svezzamento ed ingrasso era stata dell' 8,48% nelle ultime 10 settimane. Questa mortalità era suddivisa in 2,64 % nella prima fase (4 - 9 settimane di vita); 3,82 % nella seconda (10 - 15 settimane di vita); e 1,83 % in ingrasso(da 16 settimane fino al macello).
Indagini di laboratorio
Sono stati sacrificati suinetti di 6 settimane di età con respirazione addominale e perdita di condizione corporale (figura 4 e video 1). Sono stati raccolti campioni per il laboratorio.

Video 1. Suinetto in ritardo di crescita e con difficoltà respiratoria
La tabella 2 riassume i risultati della necroscopia e del laboratorio. Le figure 5, 6, 7 e 8 mostrano quanto osservato alla necroscopia.
Tabella 2. Risultati del laboratorio di 2 suinetti di 6 settimane di età in svezzamento.
| Suinetto | Necroscopia | Batteriologico | Biomolecolare | Istopatologico | ||
| 1 | Cattiva condizione corporale. Basso peso. Pericarditi, Pleuriti. Epatizzazione polmonare dell'area ventrale e dei lobi cardiaci e diaframmatico con polmonite interstiziale. | Pasteurella multocida (polmone). Streptococcus suis sierotipo 3 (polmone). |
Negativo al Mycoplasma hyopneumoniae, Virus influenza tipo A e PCV-2 mediante RT-PCR (polmone). EU-PRRS positivo mediante RT-PCR (CT: 21.2) pool di 2 polmoni dei 2 suinetti. |
Bronchi con granulociti neutrofilici ed iperplasia dell'epitelio bronchiale. Il tessuto polmonare mostra distinte fasi di broncopolmonite fibrinosa. Per cui si rileva con frequenza, epatizzazione e carnificazione. Nello spazio interlobulare ed interalveolare è presente proliferazione di tessuto fibroso multifocale. I referti indicano infiammazione cronica. | ||
| 2 |
Pleuriti. Consolidazione polmonare dell'area ventrale dei lobi cardiaco e diaframmatico con polmonite interstiziale. |
Pasteurella multocida (polmone). |
Negativo a Mycoplasma hyopneumoniae, Virus influenza tipo A e PCV-2 mediante RT-PCR (polmone). |
Segni di infiammazione cronica dei polmoni. L'infiammazione è prevalentemente di tipo cattarrale-purulenta. I bronchi sono ripieni di neutrofili e l'epitelio bronchiale è iperplasico. La cronicità si caratterizza per la proliferazione di tessuto fibroso negli spazi interstiziali. La pleura è fuocalmente iperplasica e si osserva edema interstiziale. |
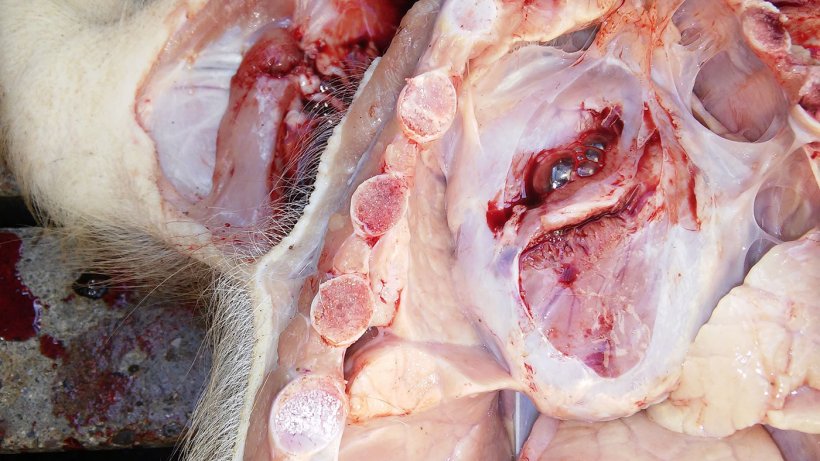
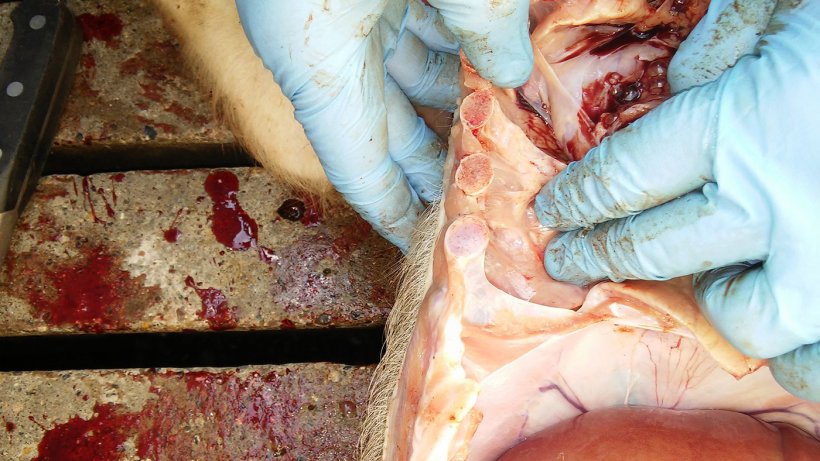

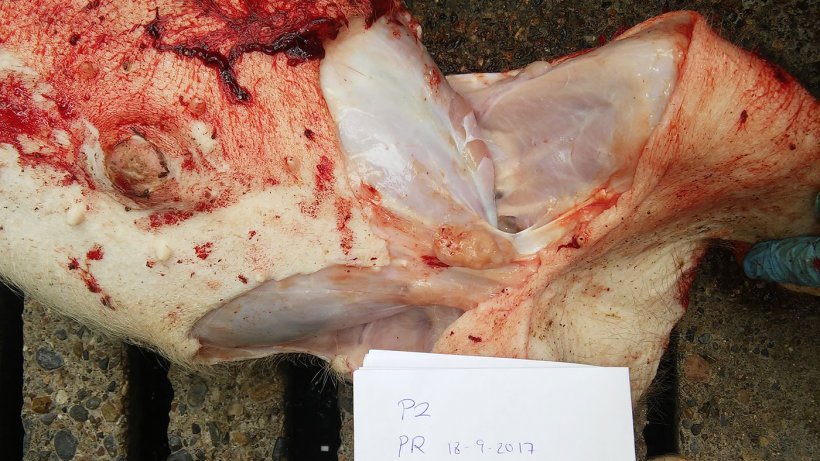
Diagnosi differenziale
In base alle indagini cliniche e di laboratorio, sono state realizzate le seguenti diagnosi differenziali:
- PRRS (Sindrome Respiratoria e Riproduttiva dei Suini).
- PCV2 (Circovirus Suino tipo 2).
- Virus Influenza tipo A.
- Polmonite Enzootica (Mycoplasma hyopneumoniae).
In base ai risultati positivi dal laboratorio, sono stati scartati gli agenti virali, come l'influenza tipo A e PCV-2. Il protocollo vaccinale nei confronti del PCV-2 era soddisfacente.
Anche la polmonite enzootica è stata scartata, sia per i risultati negativi dal laboratorio, sia per il programma vaccinale e anche per la mancanza di tosse in ingrasso.
In base allo storico ed ai risultati di laboratorio, si pensò alla PRRS assieme ad un'infezione batterica secondaria.
Programma di controllo
Si suggerì la vaccinazione con vaccinio MLV-PRRS dei suinetti a 10 – 14 giorni di età.
Risposta del programma di controllo
Ci fu una riduzione dei problemi respiratori e del numero di suinetti in ritardo di accrescimento. 3 mesi dopo, la mortalità si era ridotta fino al 5,2 %; così suddivisa: 2,25 % nella prima fase (4 a 9 settimane di vita); 1,72 % nella seconda (10 a 15 settimane); e 1,24 % in ingrasso (dalla 16sima settimana fino al macello) (figura 10). La densità non si modificò.
Discussione
Alla fine degli anni 80, sono stati descritti gravi disordini riproduttivi e respiratori negli USA (Keffaber 1989). Allora, l'agente eziologico era sconociuto. Nel 1990 è stata descritta la stessa sindrome in Germania 1990 (OIE 1992). Nel 1991 fu isolato l'agente eziologico in Olanda (Wensvoort et al. 1991) e fu chiamata Sindrome Respiratoria e Riproduttiva dei Suini (Terpstra et al. 1991).
L'infezione PRRS fu diagnosticata per la prima volta in Irlanda del Nord nel 1997 (anonimo, 1997) e nella Repubblica Irlandese nel 1999 (Ohlinger et al.2000).
La PRRS si trova nella maggior parte dei paesi produttori al mondo, con rare eccezioni: Svezia (Carlsson et al. 2009), Norvegia(OIE 1997), Finlandia (Bøtner 2003), Svizzera (Corbellini et al. 2006), Nuova Caledonia (OIE 1996), Nuova Zelanda (Motha et al. 1997), Australia (Garner et al. 1997), Argentina (Perfumo e Sanguinetti 2003), Brasile (Ciacci-Zanella et al. 2004) e Cuba (Alfonso e Frias Lepoureau 2003).
La gravità dell'infezione da PRRSv varia negli allevamenti. Agenti non infettivi possono aumentare l'espressione clinica della malattia. Questi fattori non infettivi consistono nel management, flusso dei suini, strutture e ambiente climatico (Zimmerman et al. 2012). Le infezioni concomitanti con agenti virali e batterici potenziano o aggiungono gravità ai sintomi clinici della PRRS (Shibata et al. 2003, Thacker et al. 1999, Borobia et al. 2014). La pleurite è una delle lesioni che si trovano nei polmoni di suini infetti con il PRRSv (Muirhead and Alexander 1997). Il BPEX (2009) ha riscontrato che l'impatto economico delle pleuriti è importante. L'aumento della prevalenza delle pleuriti era associato ad una riduzione del peso della carcassa e aumento dell'età alla macellazione. Il costo al produttore, con una prevalenza tipica del 10 % di pleuriti è valutato di circa £2,26 (2,59 €) per suino.
La vaccinazione con MLV PRRS ha dimostrato essere utile per limitare gli effetti del virus di campo sui suinetti svezzati (Waddell et al. 2008), come si è visto in questo caso clinico.






